Вы являетесь медицинским работником? Для полного доступа к медицинской информации войдите или зарегистрируйтесь.
Клинические инструменты оценки прогноза у пациентов с диффузной В-крупноклеточной лимфомой (ДВКЛ)
Повышение эффективности лечения первичных больных c ДВКЛ возможно при персонализированном подходе к терапии пациента.
Клинические инструменты оценки прогноза у пациентов с ДВКЛ

Самарина Светлана Валерьевна
к.м.н., заведующая клинико-диагностическим отделением гематологии и химиотерапии с дневным стационаром ФГБУН КНИИГиПК ФМБА России
Цель терапии диффузной В-крупноклеточной лимфомы (ДВКЛ) – достижение длительной ремиссии после первой линии терапии для благоприятного долгосрочного прогноза¹.
Повышение эффективности лечения первичных больных c ДВКЛ возможно при персонализированном подходе к терапии пациента. Основным и доступным в рутинной клинической практике подходом к индивидуализации терапии является определение прогноза течения заболевания для каждого пациента с целью назначения риск-адаптированной терапии в первой линии.
Для прогнозирования течения ДВКЛ используют различные шкалы оценки рисков. Одной из таких шкал является международный прогностический индекс/International Prognostic Index (МПИ/IPI), который используется в клинической практике более 25 лет и продолжает сохранять свою актуальность. Выделение групп риска ассоциировано с разной выживаемостью больных ДВКЛ. Например, пациенты высокого промежуточного и высокого риска (IPI 3–5) представляют собой наиболее сложную группу, так как для них прогноз общей выживаемости остается неблагоприятным. Для пациентов этой группы особенно актуально внедрение новых эффективных подходов терапии первой линии для достижения лучших клинических результатов.3
IPI рассчитывается по системе баллов и включает в себя параметры3:
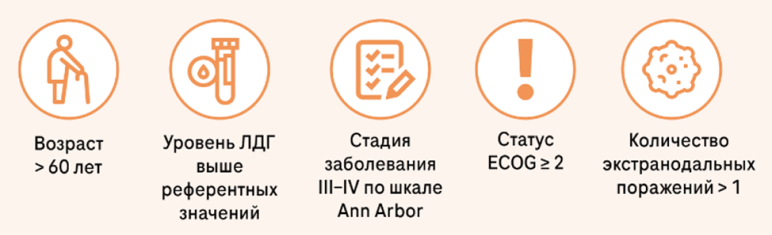
В зависимости от суммы набранных параметров выделяют 4 группы риска:
- низкий (IPI 0-1)
- промежуточный низкий (IPI 2)
- промежуточный высокий (IPI 3)
- высокий (IPI 4-5)
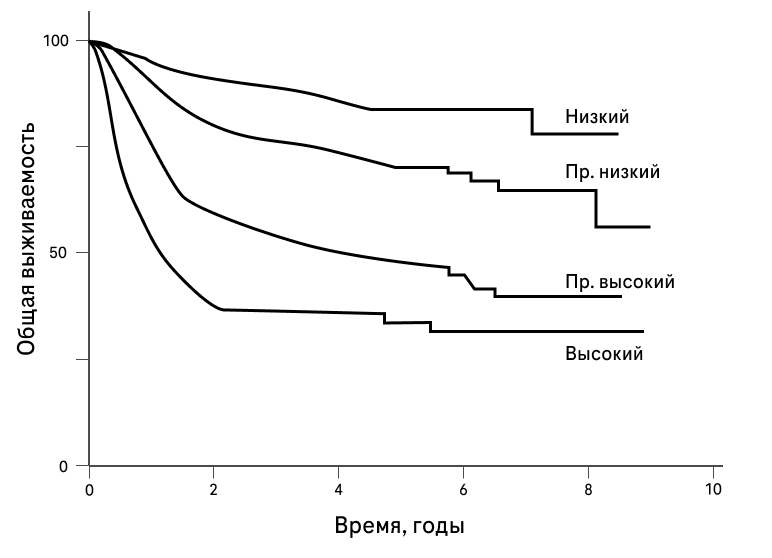
В зависимости от группы риска 5-летняя общая выживаемость (ОВ) составляет 73%, 51%, 43% и 26%, соответственно (рисунок 1)3. Таким образом, для увеличения выживаемости пациентов с наибольшим риском прогрессси по шкале IPI (IPI 3-5) представляется особенно актуальным переосмысление терапевтических подходов.
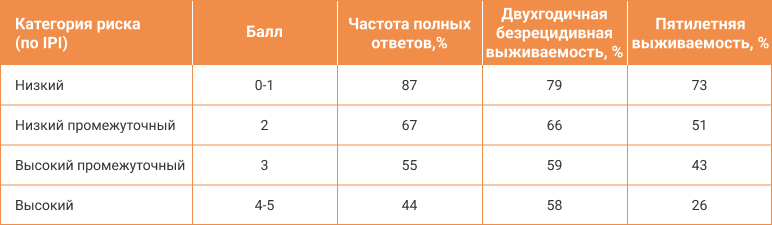
Применение терапии по схеме R-СНОР в настоящий момент нередко используется в терапии первой линии пациентов с ДВКЛ. Вместе с тем, имеются клинические данные, свидетельствующие о снижении эффективности схемы R-CHOP при значении индекса IPI более 2 баллов. При IPI >2 ОО (общий ответ) был достигнут у 79,3% пациентов, ПО (полный ответ у 51,7%, в то время как у пациентов с IPI≤2 ОО составлял 96,2%, ПО — 81,1%)5.
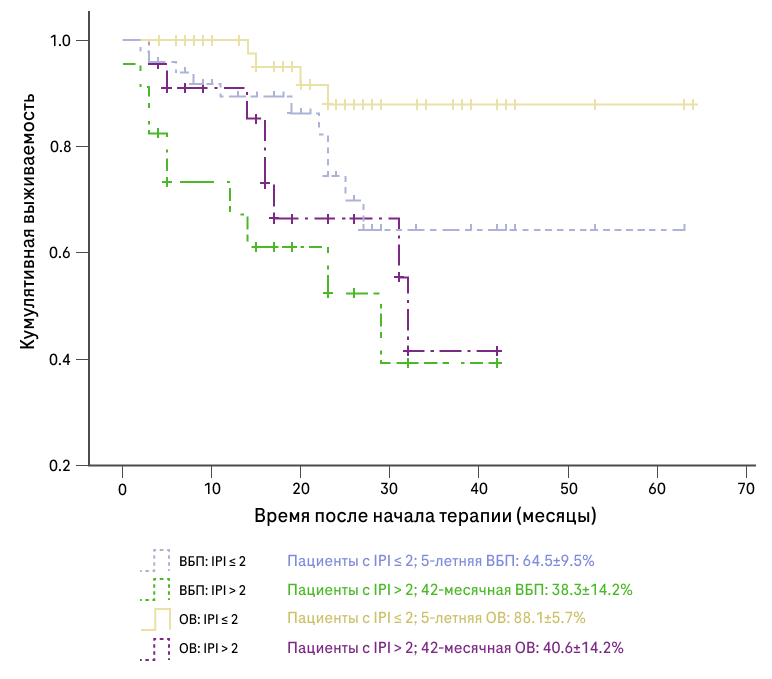
В эпоху применения ритуксимаба была разработана шкала R-IPI (пересмотренный Международный прогностический индекс, Revised IPI),которая позволяет как планировать тактику лечения, так и интерпретировать результаты клинических исследований2,24. В R-IPI включены схожие клинические и биохимические параметры, что и в шкалу IPI3,6,7.
Прогностическая шкала R-IPI

Также рассмотрим некоторые другие прогностические шкалы: NCCN-IPI и GELTAMO-IPI2,23.
Прогностическая шкала NCCN-IPI

NCCN-IPI включает в себя 5 факторов: возраст, активность ЛДГ, поражение более 1 экстранодальной зоны, стадия по классификации Ann-Arbor и соматический статус по шкале ECOG, при этом больные по возрасту разделяются на 4 группы, показатели ЛДГ — на две8.
Этими дополнениями NCCN-IPI отличается от предыдущих вариантов IPI. Модифицированный NCCN-IPI вносит уточнения в подгруппы высокого и низкого рисков в сравнении со стандартным шкалами: 5-летняя ОВ составляет 33% и 96%, соответственно. Результаты подтверждены на когорте из 1138 больных гематологами национального онкологического общества США8.
Система оценки прогноза GELTAMO-IPI основана на включении бета-2-микроглобулина (β2-MГ) в NCCN-IPI с исключением экстранодальных зон поражения в качестве прогностического фактора23. В данной прогностической шкале большое внимание в определении прогноза уделяется β2-MГ, увеличение которого отмечается примерно в 40% случаев. По результатам исследования доказано, что чем выше уровень β2-MГ, тем хуже прогноз течения болезни21.
Прогностическая шкала GELTAMO-IPI

По данным литературы, существуют дополнительные факторы, которые могут оказывать независимое влияние на прогноз течения заболевания, ОВ и БРВ (безрецидивную выживаемость) при ДВКЛ. К ним относятся B-симптомы, поражение экстранодальных органов, индекс массы тела, гематологические, биохимические показатели и молекулярно-генетические факторы9,10. При поражении ЦНС можно использовать шкалу CNS-IPI25. Вовлечение CNS при ДВКЛ встречается редко и традиционно считается неблагоприятным фактором течения заболевания11-13. Рецидивы ДВКЛ с поражением ЦНС чаще возникают при вовлечении экстранодальных органов таких, как яички, матка, почки, надпочечники и костный мозг14.
Прогностическая шкала CNS-IPI

В настоящей статье были рассмотрены наиболее часто встречающиеся клинические индексы — IPI, R-IPI, NCCN-IPI, GELTAMO-IPI, CNS-IPI. Несмотря на многообразие имеющихся подходов, необходимо отметить, что главной целью применения шкалы IPI и других, созданных на ее основе систем, является стратификация пациентов с определением тех из них, кто имеет наибольший риск прогрессирования. Подобная стратификация необходима для пересмотра подходов к терапии пациентов в пользу риск-адаптированной стратегии. Применение подхода R-CHOP в первой линии демонстрирует недостаточную эффективность у порядка 40% пациентов26. Для пациентов этой группы особенно важно применение новых подходов терапии первой линии для достижения лучших клинических результатов, что может способствовать увеличению шанса на излечение у большего числа пациентов с ДВКЛ.
Вам может быть интересно:
ДВКЛ- Диффузная В-крупноклеточная лимфома; БПВ — беспрогрессивная выживаемость; ОВ — общая выживаемость; ОО — общий ответ; ПО — полный ответ; β2-MГ — бета-2-микроглобулина; CNS (Central nervous system) ЦНС- центральная нервная система; IPI (International Prognostic Index) — международный прогностический индекс (МПИ); ЛДГ — лактатдегидрогиназа; БРВ — безрецидивная выживаемость.
Список литературы:
- Sara Ekberg et al., British Journal of Cancer volume 127, pages1642–1649 (2022)
- Prognostic molecular biomarkers in diffuse large B-cell lymphoma in the rituximab era and their therapeutic implications / Sotirios G Papageorgiou, Thomas P Thomopoulos, et al / Review Ther Adv. Hematol. / May 2021.
- Shipp, M., The International NonHodgkin’s Lymphoma Prognostic Factors Project: a predictive model for aggressive non-Hodgkin’s lymphoma / М. Shipp, D. Harrington , J. Anderson et al. // N Engl J Med. — 1993. — Vol. 329. — P. 987-994.
- Bellas, C. Immunohistochemical and molecular characteristics with prognostic significance in diffuse large B-cell lymphoma. / C. Bellas, D. Garcia, Y. Vicente, et al. // PLoS One. — 2014. — Vol. 9 (6). — P. 98169.
- Li, J. Rituximab in combination with CHOP chemotherapy for the treatment of diffuse large B cell lymphoma in Chinese patients / J. Li, L. Wang, Y. Shen et al. // Annals of Hematology September. — 2007. — Vol. 86 (9). — P. 639-645.
- Sehn, L.H. The revised International Prognostic Index (R-IPI) is a better predictor of outcome than the standard IPI for patients with diffuse large B-cell lymphoma treated with R-CHOP / L.H Sehn, В. Berry, М. Chhanabhai, С. Fitzgerald, et al. // Blood. — 2007. — Mar 1. — Vol. 109 (5). — P. 1857-61.
- Rosenberg, S.A. Validity of the Ann Arbor staging classification for the non-Hodgkin’s lymphomas. / S.A. Rosenberg // Cancer Treat Rep. — 1977. — Vol. 61 (6). — P. 1023-7.
- Zhou, Z, An enhanced International Prognostic Index (NCCN-IPI) for patients with diffuse large B-cell lymphoma treated in the rituximab era / Z. Zhou, L. Sehn, A. Rademaker, et al. // Blood. — 2014. — Vol. 123(6). — P. 837-42.
- Wight, J. Prognostication of diffuse large B-cell lymphoma in the molecular era: moving beyond the IPI. / J. Wight, G. Chong, E. Hawkes. et al. // Blood Revievs. — 2018 Sep. — Vol. 32 (5). — P. 400-415.
- El-Galaly, T.C. The number of extranodal sites assessed by PET/CT scan is a powerful predictor of CNS relapse for patients with diffuse large B-cell lymphoma: An international multicenter study of 1532 patients treated with chemoimmunotherapy. / T.C. El-Galaly, D.Villa, T.Y. Michaelsen, et al. // Eur J Cancer. — 2017. — Vol. 75. — P.195-203.
- Cai, Q.Q. New risk factors and new tendency for central nervous system relapse in patients with diffuse large B-cell lymphoma: a retrospective study. / Q.Q. Cai, L.Y. Hu, Q.R. Geng, et al. // Chin J. Cancer. — 2016. — Vol. 35 (1) 87.
- Fletcher, C.D. Central nervous system involvement in diffuse large B-cell lymphoma: an analysis of risks and prevention strategies in the post-rituximab era. / C.D. Fletcher, B.S. Kahl. // Leuk Lymphoma. — 2014. — Vol. 55 (10). — P. 2228-40.
- Kanemasa, Y. Central nervous system relapse in patients with diffuse large B cell lymphoma: analysis of the risk factors and proposal of a new prognostic model. / Y. Kanemasa, T. Shimoyama, Y. Sasaki, et al. // Ann Hematol. — 2016. — Vol. 95 (10). — P. 1661-9.
- El-Galaly, T.C. Uterine, but not ovarian, female reproductive organ involvement at presentation by diffuse large B-cell lymphoma is associated with poor outcomes and a high frequency of secondary CNS involvement. / T.C. El-Galaly, C.Y. Cheah, M. Hutchings, et al. // Br J. Haematol. — 2016. — Vol. 175 (5). — P. 876-83.
- Campbell, J. The prognostic impact of bone marrow involvement in patients with diffuse large cell lymphoma varies according to the degree of infiltration and presence of discordant marrow involvement. / J. Campbell, JF. Seymour, J. Matthews J, et al. // Eur J Haematol. — 2006. — Vol. 76 (6). — P. 473-80.
- Kim, D.H. Absolute lymphocyte counts predicts response to chemotherapy and survival in diffuse large B-cell lymphoma. / D.H. Kim, J.H. Baek, Y.S. Chae, et al. // Leukemia. — 2007. — Vol. 21 (10). — P. 2227-30.
- Cox M. Low absolute lymphocyte count is a poor prognostic factor in diffuse large B-cell-lymphoma. / M. Cox, I. Nofroni, L. Ruco, et al. // Leuk Lymphoma. — 2008. — Vol. 49 (9). — P. 1745-51.
- Wang, J. Lymphocyte-to-monocyte ratio is associated with prognosis of diffuse large B-cell lymphoma: correlation with CD163 positive M2 type tumor-associated macrophages, not PD-1 positive tumor-infiltrating lymphocytes. / J. Wang, К. Gao, W. Lei, et al. // Oncotarget. — 2017. — Vol.8 (3). — P. 5414-25.
- Oki, Y. Low absolute lymphocyte count is a poor prognostic marker in patients with diffuse large B-cell lymphoma and suggests patients’ survival benefit from rituximab. / Y. Oki, K. Yamamoto, H. Kato, et al. // Eur J Haematol. — 2008. — Vol. 81 (6). — P. 448-53.
- Judd, J. Low level of blood CD4 (+) T cells is an independent predictor of inferior progression-free survival in diffuse large B-cell lymphoma. / J. Judd, E. Dulaimi, T. Li, M. Millenson, et al. // Clin Lymphoma Myeloma Leuk. — 2017. — Vol. 17 (2). — P.83-8.
- Kanemasa, Y. Beta-2 microglobulin as a significant prognostic factor and a new risk model for patients with diffuse large B-cell lymphoma. / Y. Kanemasa, T. Shimoyama, Y. Sasaki, et al. // Hematol Oncol. — 2017. — Vol. 35 (4). — P. 440-446.
- Miyashita, K. Beta-2 microglobulin is a strong prognostic factor in patients with DLBCL receiving R-CHOP therapy. / K. Miyashita, N. Tomita, M. Taguri, et al. // Leuk Res. — 2015. — S0145-2126 (15). — 30368-4.
- Montalban, C. Validation of the NCCN-IPI for diffuse large B-cell lymphoma (DLBCL): the addition of beta2 -microglobulin yields a more accurate GELTAMO-IPI. / C. Montalban, A. Diaz-Lopez, et al. // Br J Haematol. — 2017. — Vol. 176 (6). — P. 918-28.
- https://ashpublications.org/blood/article/109/5/1857/23212/The-revised-International-Prognostic-Index-R-IPI
- https://rusoncohem.ru/klinrec/agressivnye-nefollikulyarnye-limfomy-proekt-2021-2022/#_Toc96601257
- Maurer MJ, et al. J Clin Oncol 2014;32:1066–73

