Новое поколение анти-VEGF терапии - фарицимаб
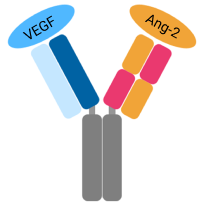 Фарицимаб (faricimab) – первое биспецифическое антитело, разработанное для интравитреального применения и первоначально называвшееся RG7716. Молекула связывает VEGF-A, с одной стороны, и ангиопоэтин-2 (Ang2) – с другой. Доклинические исследования показали, что блокирование ангиопоэтина-2 снижает вызванное VEGF разрушение эндотелиального барьера2,3. Так же было показано, что комбинированное ингибирование VEGF-A и Ang-2 снижает количество и площадь неоваскулярных поражений, препятствует лейкоцитарной инфильтрации сетчатки и уменьшает проницаемость сосудистой стенки.2
Фарицимаб (faricimab) – первое биспецифическое антитело, разработанное для интравитреального применения и первоначально называвшееся RG7716. Молекула связывает VEGF-A, с одной стороны, и ангиопоэтин-2 (Ang2) – с другой. Доклинические исследования показали, что блокирование ангиопоэтина-2 снижает вызванное VEGF разрушение эндотелиального барьера2,3. Так же было показано, что комбинированное ингибирование VEGF-A и Ang-2 снижает количество и площадь неоваскулярных поражений, препятствует лейкоцитарной инфильтрации сетчатки и уменьшает проницаемость сосудистой стенки.2
Безопасность и эффективность фарицимаба изучались в исследованиях 3 фазы: YOSEMITE&RHINE4,5 при ДМО и TENAYA&LUCERNE6,7 при нВМД.
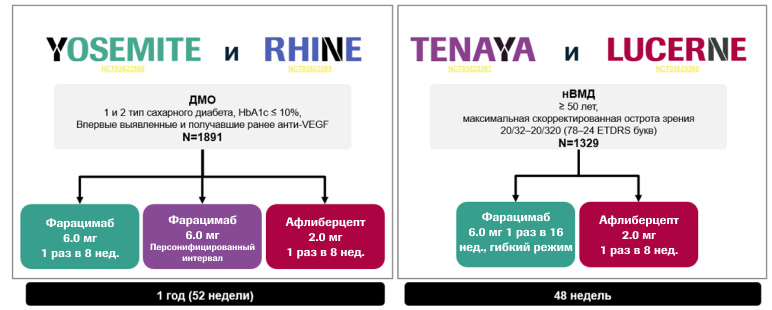
Два идентичных исследования 3 фазы YOSEMITE&RHINE6,7 оценивали эффективность, безопасность и длительность действия фарицимаба в сравнении с афлиберцептом, как у пациентов, ранее не получавших терапию, так и у пациентов, получавших ранее лечение анти-VEGF при ДМО. В исследованиях фарицимаб достиг первичной конечной точки, а именно не меньшей эффективности по сравнению с афлиберцептом в показателях МКОЗ относительно исходного уровня через год терапии. Также была продемонстрирована продолжительность действия Q16W в течение года. Более 70% пациентов получали фарицимаб с интервалом Q12W на 52 неделе терапии, а более 50% пациентов получали интервал Q16W. Фарицимаб хорошо переносился, частота ВГВ была низкой и в среднем составила 1,3% в группе фарицимаба и 0,6% в группе афлиберцепта. Случаев ретинального васкулита выявлено не было.
Два идентичных исследования 3 фазы TENAYA&LUCERNE6,7 оценивали эффективность, безопасность и длительность действия фарицимаба в сравнении с афлиберцептом у пациентов, ранее не получавших терапию анти-VEGF при нВМД. В исследованиях фарицимаб достиг первичной конечной точки, а именно стабильное улучшение МКОЗ и значимое уменьшение ТЦЗС относительно исходного уровня через год терапии фарицимабом с интервалом Q16W в сравнении с терапией афлиберцептом с интервалом Q8W. Также была продемонстрирована продолжительность действия Q16W к 48 неделе. Приблизительно 75% пациентов получали фарицимаб с интервалом Q12W, а 45% пациентов сохранили интервал Q16W. Фарицимаб хорошо переносился, частота ВГВ была низкой и в среднем составила 1,9% в группе фарицимаба и 1,2% в группе афлиберцепта. Случаев ретинального васкулита выявлено не было.
В настоящее время существует определенная проблема в ведении пациентов с патологией сетчатки, обусловленная способом доставки лекарственных средств, а также необходимостью регулярного мониторинга, что требует частых визитов в специализированное лечебное учреждение.

Список литературы
- International Council of Ophthalmology, Guidelines for Diabetic Eye Care, 2017.
- Khan M, et al. Targeting Angiopoietin in retinal vascular diseases: A literature review and summary of clinical trials involving faricimab. Cells. 2020;9:1869.
- Saharinen P et al, Nat Rev Drud Discov 2017; 16(9):635-661
- Clinical Trials.gov. A study to evaluate the efficacy and safety of faricimab (RO6867461) in participants with diabetic macular edema (YOSEMITE) [Internet; cited 2021 February]. Available from: https://clinicaltrials.gov/ct2/show/NCT03622580
- Clinical Trials.gov. A study to evaluate the efficacy and safety of faricimab (RO6867461) in participants with diabetic macular edema (RHINE) [Internet; cited 2021 February]. Available from: https://clinicaltrials.gov/ct2/show/NCT03622593
- Clinical Trials.gov. A study to evaluate the efficacy and safety of faricimab in participants with neovascular age-related macular degeneration (TENAYA) [Internet; cited 2021 February]. Available from: https://clinicaltrials.gov/ct2/show/NCT03823287
- Clinical Trials.gov. A study to evaluate the efficacy and safety of faricimab in participants with neovascular age-related macular degeneration (LUCERNE) [Internet; cited 2021 February]. Available from: https://clinicaltrials.gov/ct2/show/NCT03823300
M-RU-M-RU-0005436 Ноябрь 2021


